روش های اندازه گیری pH
الکترودهای pH چگونه کار می کنند؟ برای اندازه گیری فعالیت یون هیدروژن یک محلول می توان از روش های بصری، فتومتریک و پتانسیومتری استفاده کرد.
روش های بصری و فتومتریک به منظور تعیین pH بر تغییرات رنگی رنگدانه های آلی خاص تکیه دارند . روش های بصری با نشانگرهای بصری مانند نوارهای آزمایش pH تکمیل می شوند، در حالی که تعیین فتومتریک شامل تابش نور از طریق نمونه و اندازه گیری جذب است.
استفاده از تعیین بصری یا فتومتریک pH محدود است. اگر محلول مورد اندازه گیری کدر یا دارای رنگ ذاتی باشد، اندازه گیری ها غیر قابل اعتماد خواهند بود.
برخی از محلولهای اندازهگیری حاوی پیوندهای شیمیایی هستند که از طریق اکسیداسیون یا کاهش نشانگرهای رنگ را از بین میبرند و نتایج نادرستی ایجاد میکنند.
روش های پتانسیومتری pH را با استفاده از پتانسیل الکتریکی الکترودهای حساس به pH به عنوان سیگنال اندازه گیری تعیین می کنند.
معایب روش های بصری و فتومتری با روش های پتانسیومتری پروب pH وجود ندارد.
تعیین پتانسیومتری pH را می توان تقریباً در هر کاربردی مورد استفاده قرار داد، زیرا سنسورهای پتانسیومتری بسیار حساس و انتخابی هستند.
بین الکترودهای هیدروژن، فلز (به عنوان مثال آنتیموان) و شیشه تمایز قائل میشود، که الکترود شیشهای رایجترین حسگر pH است.
پروب های pH چگونه کار می کنند؟ پروب pH شیشه ای نمونه ای از الکترود انتخابی یونی (ISE) است.
این سیستم اندازه گیری اساساً شامل واکنش ISE بر روی یک نوع یون خاص، در این مورد، یون هیدروژن، و یک الکترود مرجع است که به طور مشترک در نمونه مورد اندازه گیری غوطه ور می شوند. ( اصول اندازه گیری pH و بهترین روش های اندازه گیری | وبینار ) را بیشتر بیاموزید .
ISE هیدروژن یک پتانسیل الکتروشیمیایی را فراهم می کند که تحت تأثیر فعالیت یون هیدروژن محلول است.
با این حال، الکترود مرجع برای ایجاد پتانسیل الکتروشیمیایی است که به ترکیب نمونه بستگی ندارد.
تفاوت بین این پتانسیل ها، ولتاژ (mV) نمایش داده شده در pH متر، مقدار pH را بر اساس معادله نرنست تعیین می کند.
ساختار و طراحی الکترود pH شیشه
یک الکترود pH معمولی از چندین ساختار منحصر به فرد تشکیل شده است که هر یک از آنها را می توان در شکل 1 مشاهده کرد.
اجزای اصلی بدنه الکترود، غشای شیشه ای حساس به pH، الکترود مرجع (یعنی سیستم مرجع)، الکترولیت مرجع و محل اتصال مرجع هستند.
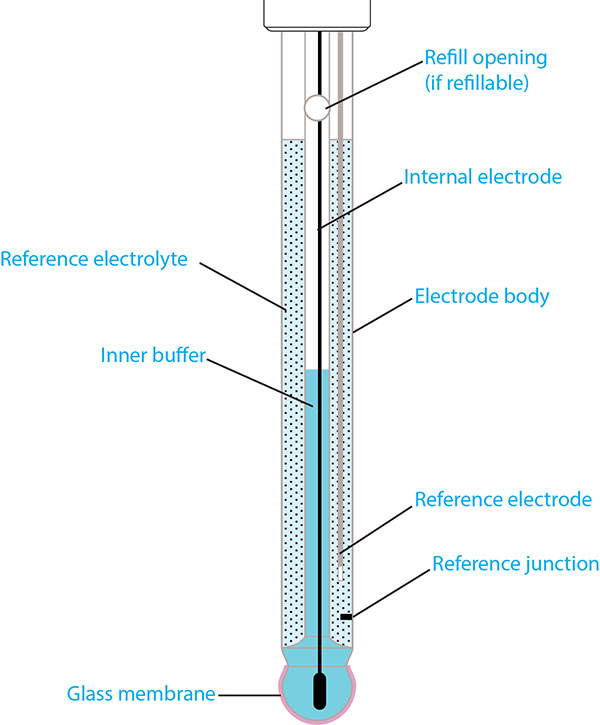
شکل 1: ساختار یک الکترود pH معمولی
بدنه الکترود
اصطلاح “الکترود شیشه ای” نشان دهنده مواد مورد استفاده برای ساخت بدنه الکترود نیست، زیرا الکترودها می توانند بدنه الکترود پلاستیکی یا شیشه ای داشته باشند. در عوض، “الکترود شیشه ای” برای توصیف مواد غشایی (یعنی غشای شیشه ای) استفاده می شود.
تمام الکترودهای میدان YSI از پلاستیک ساخته شده اند، زیرا الکترودهای بدنه پلاستیکی ناهموارتر و کمتر از شیشه شکسته می شوند.
YSI الکترودهای بدنه شیشه ای و پلاستیکی را برای آزمایشگاه ارائه می دهد، با الکترودهای شیشه ای که معمولاً دارای محدوده دمایی بیشتری هستند.
کاوشگرهای pH میدان YSI همیشه کاملاً پلاستیکی نیستند.
ماژول سنجش pH در حسگرهای PH ProDSS و EXO پلاستیکی است، اما بقیه بدنه الکترود از تیتانیوم ساخته شده است تا از دوام در میدان اطمینان حاصل شود.
یک حسگر ProDSS pH/ORP را می توان در شکل 2 مشاهده کرد.

شکل 2: سنسور pH/ORP YSI ProDSS
غشای شیشه ای
با الکترود شیشه ای، یک غشای شیشه ای به عنوان سنسور pH ذوب می شود. این غشاء با محلول بافری با pH شناخته شده (معمولاً pH = 7) پر می شود.
این طراحی الکترود محیطی با اتصال ثابت یون های H+ در داخل غشای شیشه ای ایجاد می کند، در حالی که قسمت بیرونی غشای شیشه ای در معرض نمونه قرار می گیرد که مقدار متغیری از یون های H+ وجود دارد.
تفاوت در یون های H+ پتانسیلی ایجاد می کند که در مقابل پتانسیل پایدار الکترود مرجع خوانده می شود.
به منظور اطمینان از مرطوب شدن بهینه غشای شیشه ای، شکل غشا می تواند متفاوت باشد.
شکلهای غشای کروی و مخروطی را میتوان برای اکثر کاربردها استفاده کرد، اما کاربردهای منحصربهفرد ممکن است به یک غشای تخصصی نیاز داشته باشد، مانند TruLine 21 با نوک نیزه برای نفوذ در محیط نیمه جامد و TruLine 27 با یک غشای صاف برای اندازهگیری سطح (شکل 3). جدول 1 یک نمای کلی از انواع مختلف غشاهای pH ارائه می دهد.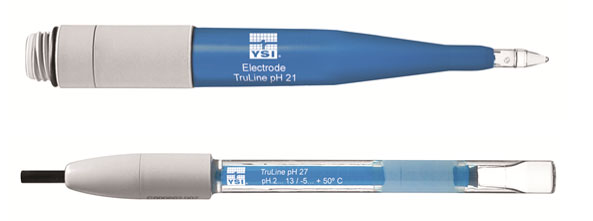
شکل 3: YSI TruLine 21 (غشاء نوک نیزه) و YSI TruLine 27 (غشاء صاف)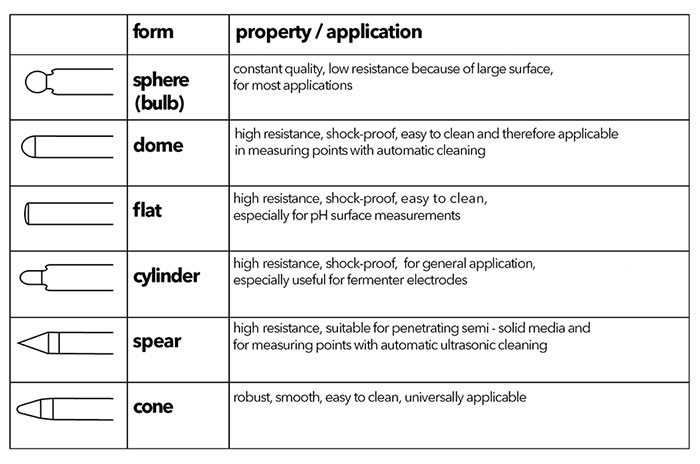
جدول 1: اشکال غشاء شیشه ای
چرا به یک مرجع نیاز است؟
اندازه گیری pH با الکترود pH شیشه ای به اندازه گیری ولتاژ متکی است. برای اندازه گیری ولتاژ دو نقطه با مقادیر پتانسیل الکتریکی متفاوت مورد نیاز است. الکترود مرجع برای حفظ پتانسیل الکتریکی ثابت طراحی شده است که مستقل از ترکیب نمونه و دما است.
در مقابل، الکترود انتخابی یون هیدروژن (ISE) با غشای شیشه ای پتانسیل الکتریکی را فراهم می کند که به فعالیت یون های هیدروژن (H+) در محلول نمونه بستگی دارد. بنابراین، هر دو الکترود مرجع و ISE هیدروژن هنگام تعیین pH مورد نیاز هستند.
انواع سیستم های مرجع
الکترود/سیستم مرجع و ISE هیدروژن (یعنی الکترود با غشای شیشه ای) می توانند الکترودهای جداگانه باشند (شکل 4) یا می توانند برای راحتی در یک الکترود واحد ترکیب شوند (شکل 1 و شکل 5).
الکترود ترکیبی بسیار رایج است و تمام الکترودهای YSI از نوع ترکیبی هستند.
صرف نظر از طراحی الکترود یا نوع سیستم مرجع مورد استفاده، الکترود مرجع در الکترولیت مرجع (معمولا KCl) غوطه ور می شود. الکترولیت مرجع با جزئیات بیشتری مورد بحث قرار خواهد گرفت.
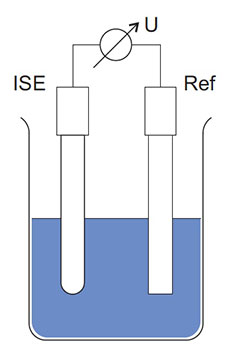
شکل 4: ساختار شماتیک یک ISE هیدروژنی، مرجع و ولت متر
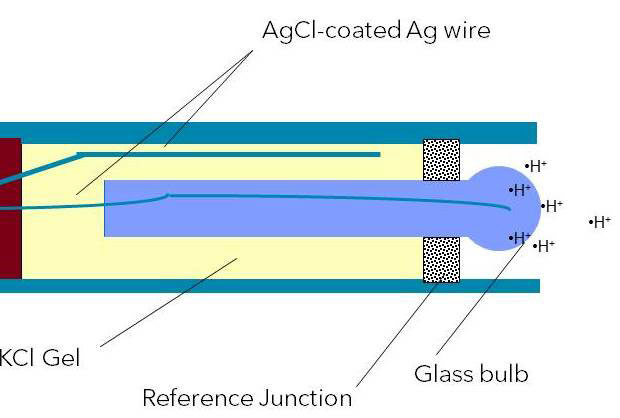
شکل 5: الکترود pH ترکیبی با الکترولیت مرجع ژل KCl
رایج ترین نوع الکترود مرجع که امروزه استفاده می شود، سیستم نقره/کلرید نقره (Ag/AgCl) است.
از آنجایی که نقره برای انسان غیر سمی است، الکترودهای Ag/AgCl را میتوان در پزشکی و فناوری غذایی که سیستمهای جیوه و تالیم سمی ممنوع هستند، استفاده کرد.
دفع نیز با Ag/AgCl کمتر از تالیم و جیوه است. Ag/AgCl دارای طیف وسیعی از کاربردها با توجه به دما (تا 140 درجه سانتیگراد) است و بنابراین برای الکترودهای قابل استریل کردن نیز مناسب است.
اکثر الکترودهای YSI دارای یک سیستم مرجع Ag/AgCl هستند.
سیستم کلرید جیوه (Hg/Hg2Cl2) برای طولانی ترین زمان مورد استفاده قرار گرفته است. این سیستم مرجع پایدارترین پتانسیل را در حضور KCl نشان می دهد.
اما امروزه به دلیل سمی بودن جیوه تنها در موارد استثنایی استفاده می شود.
همچنین، محدوده دمای قابل اعتماد هنگام استفاده از کلرید جیوه نسبتاً باریک است. در دمای بالاتر از 60 درجه سانتیگراد Hg2Cl2 شروع به تجزیه می کند.
سیستم ید/یدید، یک سیستم مرجع نسبتا جدید با زمان پاسخ سریع، اخیرا توسعه یافته است.
در مقایسه با الکترودهای معمولی با سیستمهای مرجع Ag/AgCl، الکترودهای دارای سیستمهای مرجع ید/یدید دارای مزیت حساسیت دمایی بسیار پایینتری هستند، زیرا ضریب دمایی این سیستم مرجع تقریباً صفر است.
سیستم ید/یدید نیز فاقد یون فلز است، این ویژگی به ویژه هنگام اندازهگیری در محلولهای بافر و پروتئین Tris مفید است.
سیستمهای مرجع با یونهای فلزی (مثلا Ag/AgCl) با این محلولها تعامل خواهند داشت و در نهایت منجر به مسدود شدن اتصال مرجع میشود.
سری پیشرفته الکترودهای pH YSI IoLine دارای سیستم مرجع ید/یدید هستند. رنگ منحصر به فرد مرجع IoLine در شکل 6 قابل مشاهده است.

شکل 6: الکترود pH YSI IoLine
خواص یک الکترولیت مرجع خوب
الکترولیت مرجع از طریق محل اتصال به نمونه متصل است، زیرا برای بستن مدار الکتریکی در الکترود عمل می کند.
یک الکترولیت مرجع خوب باید ویژگی های خاصی داشته باشد. الکترولیت مرجع باید رسانایی الکتریکی خوبی داشته باشد و از نظر شیمیایی خنثی باشد.
از آنجایی که معمولاً مقداری الکترولیت در طول اندازهگیری به نمونه نشت میکند، همچنین مهم است که الکترولیت با محلول اندازهگیری واکنش نشان ندهد.
یون های محلول الکترولیت نیز باید به همان اندازه متحرک باشند. اگر یونها در محلول الکترولیت با سرعتهای متفاوتی منتشر شوند، یک پتانسیل الکتریکی (یعنی پتانسیل انتشار ) میتواند به دلیل تقسیم بین بار مثبت و منفی تشکیل شود.
این پتانسیل ناخواسته هنگام اندازه گیری pH می تواند بسیار مشکل ساز باشد.
با برخی از یون ها (به عنوان مثال K + و Cl – )، تفاوت در سرعت انتشار اندک است، که منجر به پتانسیل انتشار بسیار کمتری می شود.
کلرید پتاسیم (KCl) همه این خصوصیات را دارد. در نتیجه، KCl رایج ترین محلول الکترولیت مورد استفاده است.
شکل الکترولیت مایع
الکترودها می توانند دارای ژل، پلیمر یا الکترولیت مایع باشند.
تمام الکترودهای میدان YSI و برخی از الکترودهای آزمایشگاهی YSI (به عنوان مثال TruLine 25 و TruLine 26 ) دارای یک الکترولیت ژل هستند، در حالی که اکثر الکترودهای آزمایشگاهی YSI دارای یک مرجع الکترولیت مایع هستند که می تواند دوباره پر شود.
الکترولیت پلیمری در الکترودهای تخصصی YSI با نوک تخت ( TruLine 27 ) و نوک نیزه ( TruLine 21 ) استفاده می شود.
الکترولیت مایع
الکترودهای دارای الکترولیت مایع معمولاً میتوانند دوباره پر شوند، بنابراین عمر الکترود طولانیتر میشود.
بنابراین، بر خلاف الکترود با الکترولیت ژل، الکترولیت را می توان به راحتی تخلیه کرد و در صورت آلوده شدن الکترولیت جایگزین کرد.
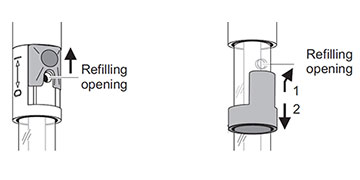
اگر از الکترود آزمایشگاهی YSI با مرجع قابل پر کردن مجدد استفاده می کنید، مهم است که به یاد داشته باشید دهانه پر کردن مجدد باید همیشه در حین کالیبراسیون و اندازه گیری باز باشد!
همچنین مطمئن شوید که سطح پر شدن الکترولیت حداقل 2 سانتی متر بالاتر از سطح محلول کالیبراسیون و/یا اندازه گیری باشد.
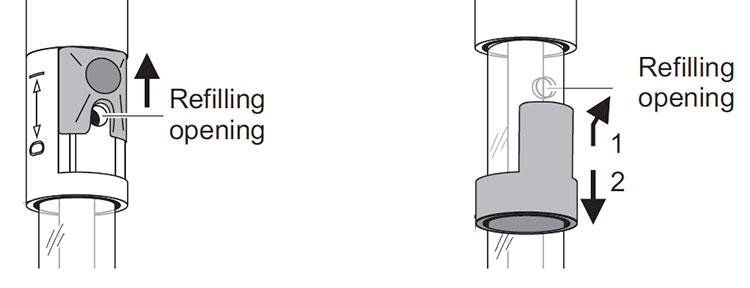
شکل 7: دهانه های کشویی (چپ) و درپوش (راست) برای الکترودهای آزمایشگاهی YSI
زمان پاسخ معمولاً با الکترودهایی که دارای الکترولیت مایع هستند سریعتر است. همچنین، الکترودهای دارای الکترولیت مایع محدودیتهای کمتری در محدوده استفاده دارند، زیرا الکترولیتهای ژل و پلیمر مقاومت کمتری در برابر تغییرات دما و دما دارند.
برخلاف الکترودهای دارای الکترولیت مایع، سرعت خروجی فوقالعاده کوچک ژل و الکترولیت پلیمری در محلولهای به شدت اسیدی، بازی و با قدرت یونی پایین میتواند منجر به خطاهای اندازهگیری به دلیل تشکیل پتانسیلهای انتشار شود.
تمام الکترودهای آزمایشگاهی قابل شارژ مجدد YSI از 3 مولار KCl برای الکترولیت مرجع استفاده می کنند. با این حال، از آنجایی که الکترولیت از طریق اتصال به نمونه متصل می شود، برخی از کاربردها به محلول های الکترولیت تخصصی نیاز دارند.

شکل 8: الکترودهای آزمایشگاهی قابل شارژ مجدد YSI (Science pHT-G و TruLine 17)
طراحی الکترود YSI IoLine امکان استفاده از الکترولیت های دیگر را فراهم می کند که نیازهای کاربرد نمونه برداری را برآورده می کند.
به عنوان مثال، اگر الکترولیت کاملاً بدون کلرید مورد نیاز است (یعنی KCl نیست)، می توان از الکترولیت پل دیگری مانند سولفات پتاسیم 0.6 مولار (K 2 SO 4 ) با IoLine استفاده کرد.
ژل و الکترولیت پلیمری
الکترولیت ژل همچنان از KCl تشکیل شده است، اما یک عامل ژل کننده به منظور جلوگیری از نشت آسان الکترولیت به نمونه از طریق اتصال مرجع در طول اندازه گیری اضافه می شود.
از آنجایی که عملاً هیچ از دست دادن الکترولیت وجود ندارد، نگهداری این الکترودها آسان تر است، زیرا نیازی به پر کردن مجدد آنها با الکترولیت نیست.
از آنجایی که نمی توان آنها را دوباره پر کرد، الکترودهای دارای الکترولیت ژل عمر کوتاه تری نسبت به الکترودهای دارای الکترولیت مایع دارند.

شکل 9: الکترود YSI TruLine pH 25 با الکترولیت ژل و بدنه پلاستیکی
الکترولیت پلیمری جامد است و می تواند در طول اندازه گیری مستقیماً با نمونه تماس بگیرد. به دلیل عدم وجود جریان الکترولیت، تحرک همه یون ها بسیار محدود است.
این منجر به عدم رسوب نقره در محل اتصال می شود و انتشار یون های خارجی در الکترود را عملا غیرممکن می کند.
الکترودهای تخصصی YSI TruLine 21 و 27 pH دارای سیستم REFERID هستند که شکل منحصر به فردی از الکترولیت پلیمری است.
این الکترودها تعمیر و نگهداری پایینی دارند و با مقاومت بالا در برابر تغییرات فشار و فشار مشخص می شوند. سیستم REFERID همچنین دارای یک ذخیره KCl قابل مشاهده است.
پیوند مرجع pH، وظیفه شما چیست؟
محل اتصال مرجع که به عنوان دیافراگم نیز شناخته می شود، تماس الکتریکی بین سیستم مرجع و محلول ایجاد می کند. مانند الکترولیت مرجع، اتصال مرجع باید دارای ویژگی های خاصی باشد.
ولتاژهای انتشار در محل اتصال یک خطای رایج اندازه گیری است، بنابراین اتصال نقش عمده ای در دقت اندازه گیری دارد. برای کوچک نگه داشتن این پتانسیل های مخرب، محل اتصال باید خروجی نسبتاً بزرگ و ثابت الکترولیت مرجع را تضمین کند.
با این حال، محل اتصال باید فقط کمی نفوذپذیر باشد تا از خروج سریع الکترولیت جلوگیری کند، که به ویژه در مورد الکترودهایی که از الکترولیت مایع استفاده می کنند مهم است. انواع مختلف اتصالات دارای نرخ خروج الکترولیت متفاوتی هستند.
علاوه بر نفوذپذیری محل اتصال، مقاومت الکتریکی آن باید تا حد امکان کم باشد و از نظر شیمیایی بی اثر باشد.
انواع اتصالات مرجع
انواع مختلفی از اتصالات وجود دارد که هر کدام ویژگی های منحصر به فردی دارند.
بسته به کاربرد، باید برای الکترودهای YSI با الکترولیت مایع تصمیم گرفت که آیا اتصال سرامیکی، زمینی یا پلاتینیومی به بهترین وجه با شرایط اندازه گیری مطابقت دارد یا خیر.
جدول 1 یک نمای کلی از انواع مختلف اتصالات، از جمله شکاف حلقوی ( TruLine 27 ) و فیبر ( TruLine 25 و TruLine 26 ، MultiLab IDS 4110 ) ارائه می دهد.
جدول 2: انواع اتصالات مرجع
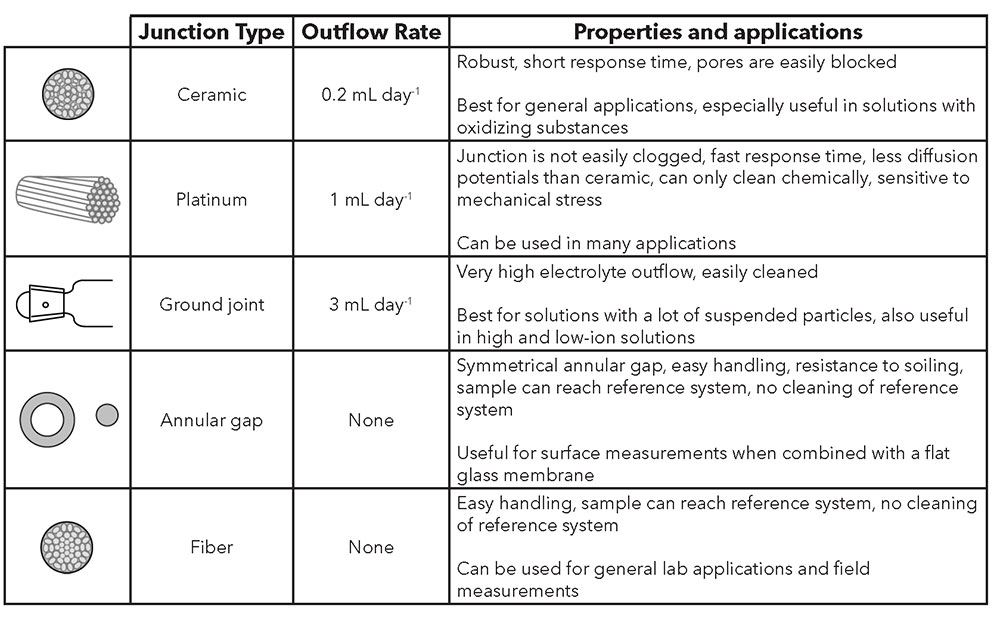
سرامیک
اتصال سرامیکی از تخلخل سرامیک بدون لعاب استفاده می کند. اتصالات سرامیکی دارای نرخ خروجی KCl ~ 0.2 میلی لیتر در روز و مقاومت الکتریکی نسبتاً بالایی (1 کیلو اهم) هستند.
پتانسیل های انتشار به راحتی در محلول های اندازه گیری با قدرت یونی بیشتر ایجاد می شود، زیرا گرادیان غلظت در محل اتصال بسیار زیاد است.
در محلول های با قدرت یونی پایین تر، مقاومت ماده آزمایشی ممکن است برای اندازه گیری های دقیق خیلی زیاد باشد.
هر دو اثر با سرعت کم خروجی تقویت می شوند، بنابراین اتصالات سرامیکی در چنین مواردی کمتر مناسب هستند. به دلیل خطر بالای مسدود شدن منافذ آن، برای محلول های حاوی ذرات معلق نیز مناسب نیست.
فقط در محلول های اندازه گیری که حاوی مواد اکسید کننده هستند، محل اتصال سرامیکی بر اتصال پلاتین برتری دارد.
پلاتین
محل اتصال پلاتین شامل رشته های پلاتین پیچ خورده و ظریفی است که بین آنها الکترولیت در امتداد کانال های دقیقاً تعریف شده به بیرون جریان می یابد.
اتصال پلاتین دارای جریان بسیار ثابتی است و به راحتی مسدود نمی شود.
با سرعت خروجی ~ 1 میلی لیتر در روز و مقاومت الکتریکی ~ 0.5 کیلو اهم، مزایایی نسبت به اتصالات سرامیکی دارد.
اتصال پلاتین به تنش های مکانیکی حساس تر است و همچنین به دلیل وقوع پتانسیل های مخرب برای محلول های به شدت اکسید کننده یا کاهش دهنده کمتر از حد مطلوب است.
با این حال، اتصال پلاتین را می توان تقریباً به طور کلی استفاده کرد.

شکل 10: الکترود TruLine pH 17 با اتصال پلاتین
زمین مشترک
اتصال زمین به اتصال زمین با شکاف نازک شیشه زمینی روغن کاری نشده به عنوان یک دهانه خروجی برای الکترولیت کار می کند. سرعت خروجی ~ 3 میلی لیتر در روز و بیشتر است.
دارای مقاومت الکتریکی بسیار پایین (0.1 کیلو اهم) است.
اتصال زمین به اتصال زمین برای اندازه گیری در محلول های آلوده مناسب است، زیرا تمیز کردن آن آسان است. به دلیل سرعت بالای خروجی، برای محلول های با یون بالا و پایین مناسب است.

شکل 11: الکترود علمی pHT-G با اتصال زمین به اتصال
پلاستیک
اتصالات ساخته شده از الیاف پلاستیکی نیز می تواند برای کاربردهای خاص استفاده شود.
به عنوان مثال، الکترودهای ترکیبی با یک شفت پلاستیکی اغلب دارای اتصالات ساخته شده از الیاف نایلونی برای جلوگیری از آلودگی سوراخ اتصال هستند.
برای اندازه گیری فرآیند در محلول هایی که حاوی فلوراید هستند، از کلیدهای الکترولیت با اتصالات PTFE استفاده می شود.


